W dniach 28 lutego i 1 marca 2023 roku w Międzynarodowym Instytucie Biologii Molekularnej i Komórkowej w Warszawie odbyło się szkolenie z zakresu etyki i rzetelności w badaniach naukowych. Szkolenie prowadziła Prof. Ana Borovečki, dyrektor Katedry Medycyny Społecznej i Organizacji Opieki Zdrowotnej w Szkole Zdrowia Publicznego na Uniwersytecie w Zagrzebiu (Chorwacja).
W dniu 28 lutego 2023 r. roku nasi naukowcy wzięli udział w sesji wykładowej dotyczącej etycznych aspektów w badaniach naukowych. Sesja obejmowała między innymi następujące tematy:
- rodzaje uchybień w badaniach naukowych,
- rzetelność prac badawczych,
- wymagania dotyczące autorstwa,
- dobre praktyki dla doktorantów i ich opiekunów.
Sesja była bardzo inspirująca i zainteresowała zarówno młodych, jak i bardziej doświadczonych badaczy. W szczególności, uczestnicy z dużym zaangażowaniem podeszli do interaktywnego instruktażu on-line.
W dniu 1 marca 2023 r. doktoranci z MIBMiK uczestniczyli w dwóch warsztatach poświęconych rzetelności badań. Prof. Borovečki omówiła i podała przykłady europejskich wytycznych dotyczących etyki w badaniach biomedycznych. Interesujące było porównanie, jak różni się podejście do kwestii etycznych w różnych częściach świata. W czasie warsztatów studenci mieli okazję do omówienia kwestii etycznych związanych z ich własnymi projektami.
Szkolenie było wspierane przez projekt MOSaIC, który otrzymał dofinansowanie z programu Unii Europejskiej Horyzont 2020 w zakresie badań i innowacji na podstawie umowy nr 810425.
{gallery}research-ethics{/gallery}
Z radością informujemy, że dr Ewelina Małecka-Grajek, Kierownik Laboratorium Biofizyki Pojedynczych Cząsteczek otrzymała finansowanie na projekt badawczy ramach konkursu SONATA BIS 12! Tytuł tego projektu brzmi: „Dynamika kompleksów degradujących RNA u bakterii” a jego finansowanie opiewa na kwotę pond 3 mln zł! Serdecznie gratulujemy! Poniżej prezentujemy opis zwycięskiego projektu.
Wszystkie procesy biologiczne zaczynając od bakterii walczących z wirusami po rozwój serca u człowieka są kontrolowane przez zmiany w ekspresji materiału genetycznego i dynamicznych oddziaływań między cząsteczkami białek i RNA. Wiemy już dużo na temat tego jak te białka wyglądają strukturalnie, jakie elementy RNA rozpoznają oraz jaki wpływa na komórkę mają takie oddziaływania lub ich brak. W ostatnich latach coraz więcej nacisku kładzie się na poznawanie mechanizmów molekularnych rządzących procesami biologicznymi. Dzięki takim badaniom możemy zrozumieć, jak mechanizmy ewoluują, ale również możemy lepiej nimi manipulować np. w rozwoju szczepionek.
Celem tego projektu jest badanie mechanizmów molekularnych rządzących komunikacją między poszczególnymi procesami takimi jak wyciszaniem RNA, degradacją RNA i translacją u bakterii. Po-transkrypcyjna regulacja genów odpowiada za reakcję bakterii na stres np. przestawienie metabolizmu na dostępne składniki odżywcze czy dostosowanie się do warunków gospodarza w przypadku patogennych szczepów. Ta regulacja jest umożliwiana przez małe RNA (sRNA) oddziałujące z informacyjnym RNA (mRNA) na zasadzie komplementarności. W parowaniu między sRNA i mRNA uczestniczy białko opiekuńcze Hfq. Związanie mRNA przez sRNA często prowadzi do degradacji obu cząsteczek, a więc obniża ekspresję docelowego mRNA. Z kolei za degradację większości RNA bakteryjnych, także tych sparowanych przez Hfq, odpowiada kompleks białkowy zwany degradosomem zawierający enzym katalizujący cięcie RNA: rybonuklazę E (RNazę E). Co ciekawe, sRNA występują w komórkach w kompleksach z Hfq, ale również Hfq i degradosomem. Nie wiadomo jakie różnice funkcjonalne dzielą te kompleksy. W skład degradosomu często wchodzi też helikaza RhlB rozplatająca ustrukturyzowane RNA, więc stawiamy hipotezę, że obecność degradosomu umożliwia dostęp sRNA do wcześniej niedostępnych miejsc w docelowych mRNA. Ponadto nie wiadomo czy utworzenie stabilnego kompleksu degradującego mRNA zależy od kolejności dołączania poszczególnych komponentów. Wcześniejsze badania wykazały, że większość, lecz nie wszystkie sRNA jest degradowana łącznie z docelowym mRNA, co doprowadziłoby również do wyciszenia regulatora. Nie jest jednak wiadomo jakie czynniki decydują o degradacji sRNA lub czy Hfq jest obecne w tym procesie. Jeśli tak, jest możliwe, że krótkie fragmenty pozostałe po degradacji RNA pozostają związane do Hfq wpływając na dalsze losy docelowych mRNA. Planujemy odtworzyć katalitycznie aktywny degradosom posiadający również zdolność do oddziaływania z białkami. Z wykorzystaniem fluorescencyjnie znakowanych komponentów, będziemy w stanie śledzić składanie kompleksów równolegle z katalizą RNA.
Dodatkowym skomplikowaniem w koordynacji tych procesów jest to, że RNA podlega ciągłej translacji. Wiadomo, że sRNA często celują w obszar wiązania rybosomu na mRNA, jednak nie jest jasne, czy dochodzi do bezpośredniej konkurencji między rybosomem a kompleksem sRNA-Hfq. Ponadto, degradosomy przeprowadzające cięcie w regionach kodujących mRNA muszą bezpośrednio koordynować pracę z rybosomami. Chcemy zwizualizować jak dynamiczne są te procesy. Badania przeprowadzone w ramach tego projektu dadzą wgląd w komunikację między kluczowymi procesami komórkowymi zaangażowanymi w ekspresję informacji genetycznej. Poznamy dynamikę tych mechanizmów w skali milisekund, a więc w realnej rozdzielczości czasowej w jakiej procesy te zachodzą w komórce. Poprzez monitorowanie pojedynczych cząsteczek otrzymamy także wgląd w heterogenność tych procesów. Te wszystkie informacje będą cenne w zaprojektowaniu sztucznych regulatorów ekspresji genów i symulowaniu ich efektów.
Z radością informujemy, że zespół prof. dra. hab. Matthiasa Bochtlera otrzymał Nagrodę Ministra Edukacji i Nauki za znaczące osiągnięcia w zakresie działalności naukowej. Dotyczą one zaawansowanych badań mechanizmów metylacji i demetylacji DNA odpowiedzialnych za stan epigenetyczny genomów. Wyniki tych badań przyczyniły się do zrozumienia mechanizmów regulujących ekspresję genów i zostały opublikowane w cyklu sześciu artykułów naukowych, m.in. w czasopiśmie Nucleic Acids Research. Nagroda została przyznana na Gali Nauki Polskiej, która odbyła się w niedzielę, 19 lutego br w Toruniu. Serdecznie gratulujemy!
Zespół pod kierunkiem prof. Matthiasa Bochtlera zajmuje się wyjaśnieniem mechanizmów wprowadzania, odczytu, usuwania, a przede wszystkim funkcji modyfikacji DNA. Metylacja DNA jest ewolucyjnie wczesnym zjawiskiem, dzięki czemu do badań można wykorzystać również proste modele prokariotyczne. Wykorzystanie systemów bakteryjnych umożliwia znalezienie i charakterystykę enzymów, które są lub mogą być używane jako narzędzia w badaniach metylacji DNA w organizmach wyższych. Prof. Bochtler wykorzystuje w badaniach biochemicznych szeroki repertuar metod od biologii strukturalnej prokariotycznych systemów modelowych, poprzez analizę chemiczną i biofizyczną, kończąc na analizie w komórkach oraz na poziomie bioinformatycznym u zwierząt. Długotrwała współpraca zespołu prof. Bochtlera z firmą biotechnologiczną NEB – kluczowym dostawcą endonukleaz restrykcyjnych stosowanych w inżynierii genetycznej – wskazuje na wysoki potencjał aplikacyjny prowadzonych badań, w tym proponowanych nowych narzędzi molekularnych. Osiągnięcia zespołu prof. Bochtlera mają nowatorski charakter i wyróżniają się bardzo szerokim podejściem do biologii strukturalnej, przyczyniając się do rozwoju tej dyscypliny.
W skład nagrodzonego zespołu wchodzą:
- prof. dr hab. Matthias Bochtler,
- dr hab. Honorata Czapińska,
- dr Humberto Fernandes,
- dr Henryk J. Korza,
- dr Monika Kowalska,
- dr Anton Slyvka,
- mgr Igor Helbrecht,
- mgr Marlena Kisiała,
- mgr Katarzyna Krakowska,
- mgr Michał Pastor
Więcej o wydarzeniu: https://www.gov.pl/web/edukacja-i-nauka/gala-nauki-polskiej



Dr Urszula Białek-Wyrzykowska, Zastępca Dyrektora ds. Rozwoju MIBMiK wzięła udział w konferencji pt. „Doskonałość naukowa nie ma płci”, zorganizowanej przez Akademię Młodych Uczonych PAN na Wydziale Nauk Politycznych i Dziennikarstwa Uniwersytetu im. Adama Mickiewicza w Poznaniu. Wystąpienie zatytułowane „Doskonałość naukowa nie ma płci – ustrukturyzowany długoletni program wyrównywania szans płci poprzez zmiany w warunkach i kulturze pracy” dotyczyło działań podejmowanych przez MIBMiK w tym obszarze. Dr Białek-Wyrzykowska przedstawiła również rekomendacje i przykłady dobrych praktyk wdrażanych w tym zakresie przez konsorcjum europejskich instytutów badawczych EU-LIFE.
Problem nierówności płci w różnych aspektach i obszarach nauki, w tym problem ukrytych uprzedzeń, prowadzących do dysproporcji pomiędzy kobietami i mężczyznami w nauce – to kwestia, która od wielu lat stanowi wyzwanie nie tylko w środowisku naukowym. Badania i raporty z analiz dotyczące tej kwestii, opublikowane m.in. przez Narodowe Centrum Nauki, Fundację na rzecz Nauki Polskiej oraz Fundację L’Oreal – wskazują jednoznacznie na potrzebę wyrównywania dysproporcji między przedstawicielami obu płci na poszczególnych szczeblach i etapach kariery naukowej.
Konferencja zorganizowana przez Akademię Młodych Uczonych PAN stanowiła doskonałą okazję do rozpoczęcia dialogu pomiędzy jednostkami naukowo-badawczymi oraz do wypracowania realnych działań służących przeciwdziałaniu odpływowi ludzi nauki z wielu obszarów badawczych. Wydarzenie to było jest skierowane do władz jednostek naukowo-badawczych, przedstawicieli Ministerstwa Edukacji i Nauki, instytucji finansujących naukę w Polsce oraz organizacji zajmujących się promowaniem nauki i badań naukowych w Polsce.
Konferencja pt. „Doskonałość naukowa nie ma płci” odbyła się 10 lutego br. Jej współorganizatorami byli: Narodowe Centrum Nauki, Centrum Badań nad Partycypacją Kobiet w Przestrzeni Publicznej Uniwersytetu im. Adama Mickiewicza w Poznaniu oraz Biuro Promocji Nauki “PolSCA” Polskiej Akademii Nauk w Brukseli.
Udział przedstawicieli MIBMiK w konferencji został sfinansowany w ramach projektu MOSaIC 

Więcej na ten temat na stronie wydarzenia: https://amu.pan.pl/dnnmp/
{gallery}excellence{/gallery}
Starzenie się organizmu to fascynujący proces biologiczny, podczas którego następuje szereg zmian w przebiegu czynności życiowych komórek oraz całego organizmu. Proces ten może wpływać na obniżenie odporności organizmu oraz zmniejszenie jego umiejętności adaptacyjnych do otaczających warunków. Czy zastanawialiście się kiedyś jak starzenie wpływa na zdolność regulowania poziomów żelaza w naszym organizmie? Czy prosta zmiana diety może poprawić wydajność obrotu żelaza u starzejących się osób? Na te pytania odpowiedzieli Patryk Ślusarczyk i Pratik Mandal oraz współpracownicy pod kierownictwem dr Katarzyny Mleczko-Saneckiej (Laboratorium Homeostazy Żelaza) oraz dr hab. Wojciecha Pokrzywy (Laboratorium Metabolizmu Białek) w najnowszym artykule czasopisma eLife.
Wraz z wiekiem nasze organizmy tracą zdolność do prawidłowej regulacji poziomów żelaza, choć mechanizmy tych zmian nie były dotąd do końca znane. Badanie naukowców z Laboratorium Homeostazy Żelaza i Laboratorium Metabolizmu Białek wykazało, że starzejąc się, makrofagi czerwonej miazgi śledziony (RPM), czyli komórki, które usuwają wadliwe czerwone krwinki, ulegają upośledzeniu i ubumierają. Prowadzi to do powstawania złogów białkowych bogatych w żelazo i hem, oraz do gromadzenia się starych i zużytych czerwonych krwinek w śledzionie. Badanie z użyciem organizmów modelowych – w tym przypadku myszy - wykazało również, że kiedy były one karmione dietą z obniżoną zawartością żelaza, makrofagi RPM były w lepszej kondycji i zdolność organizmu do ‘recyklingu żelaza’ poprawiła się.
Odkrycie to sugeruje, że redukcja żelaza w diecie może być potencjalną strategią utrzymania prawidłowej homeostazy żelaza podczas starzenia. Dostarcza również nowych informacji na temat zależności między starzeniem a homeostazą żelaza i może stanowić podstawę do przyszłych badań dotyczących poprawy zdrowia w populacji starszych osób.
Cały artykuł dostępny pod linkiem: https://elifesciences.org/articles/79196

Międzynarodowy Instytut Biologii Molekularnej i Komórkowej w Warszawie ogłasza nabór na stanowiska Kierowników Laboratoriów. Zapraszamy do zapoznania się z ofertą.
The IIMCB is an internationally recognized research institute in Poland where cutting-edge research meets innovation. In line with the IIMCB’s mission, we support ambitious scientists of any nationality to pursue frontier research to respond to health-related societal challenges. We are looking for talented, dynamic, and motivated scientists to establish their first independent research groups. Successful candidates will be supported by the IIMCB’s institutional project entitled “RNA and Cell Biology - from Fundamental Research to Therapies” (RACE) selected for funding in the Teaming for Excellence programme under Horizon Europe. The prospect of a new, larger building with state-of-the-art infrastructure offers the new groups an unprecedented opportunity for scientific and personal development.
The IIMCB hosts a vibrant, multinational community of scientists and is well connected internationally, as exemplified by the composition of the IIMCB’s International Advisory Board and the IIMCB’s membership in the EU-LIFE, an alliance of 15 top independent European research institutes. The IIMCB has an excellent record of attracting funding on national and international levels, and a high proportion of EMBO members among its group leaders.
Candidates’ profile:
Successful candidates must have an outstanding record of scientific accomplishments and be able to develop an independent competitive research program in one of the following areas: (i) RNA biology: drug development, including chemical biology and formulations for RNA therapeutics; (ii) cell biology: tissue, organoid, and animal models of human diseases, modification of patient-derived cells for development of cell-based therapies, (iii) computational biology: AI/machine learning approaches, big data analysis, and advanced bioinformatics.
The proposed program is expected to broaden the scope of and synergize with research performed at the IIMCB (see more at www.iimcb.gov.pl).
The IIMCB offers:
- Junior Group Leader position (a full-time salary with social benefits), with an initial appointment
of 5 years and possible subsequent promotion to a position with rolling tenure upon positive evaluation - Start-up funds and core funding after the start-up funds have been used
- Access to state-of-the-art equipment
- Support in applying for national and international grants
- Full organizational and administrative support by professional English-speaking staff
- Friendly, inclusive, international working environment
- Access to the International PhD program of the IIMCB
Applications should include:
- Cover letter explaining motivation for application
- Curriculum Vitae including a publication list
- Concise statement of 1-3 scientific achievements
- Two-page summary of research plans
- Contact information for two references
How to apply:
- Applications should be sent to Ten adres pocztowy jest chroniony przed spamowaniem. Aby go zobaczyć, konieczne jest włączenie w przeglądarce obsługi JavaScript.
- In the subject of the message include "JGL" and your first and last name
- Please include the following statement in your CV: “I hereby agree to the processing of my personal data, included in the application documents by the International Institute of Molecular and Cell Biology
in Warsaw, 4 Księcia Trojdena Street, 02-109 Warsaw, for the purpose of carrying out thecurrent recruitment process.” Your personal data will be processed for the purpose of the recruitment procedure by the International Institute of Molecular and Cell Biology in Warsaw. Full information is available under the link https://bit.ly/3UFWpY2.
The deadline for applications is March 31, 2023. Chosen applicants will be asked to give on-line lectures on
May 11-17, 2023. Short-listed applicants will be invited for on-site interviews during the IIMCB’s International Advisory Board meeting on June 19-21, 2023. The positions are available from September 2023 with the formal appointment date set on a case-by-case basis.
Inquiries about the offer, research environment, and science in Poland are welcome and should be sent
to Ten adres pocztowy jest chroniony przed spamowaniem. Aby go zobaczyć, konieczne jest włączenie w przeglądarce obsługi JavaScript..
All information provided by applicants will remain strictly confidential and will be reviewed only by authorized officials of the selection committee.


W tym tygodniu, 23-27.01.2023, w Międzynarodowym Instytucie Biologii Molekularnej i Komórkowej w Warszawie odbył się kurs krytycznego czytania publikacji naukowych (Critical Reading of Scientific Papers), który składał się z 2 wykładów i 3 warsztatów. Zarówno kurs, jak i idea jego organizacji spotkała się z dużym zainteresowaniem ze strony uczestników, którzy wysoko ocenili jego wartość, podkreślając, że śledzenie i recenzowanie literatury naukowej jest bardzo istotną częścią ich pracy.
Wykłady online prowadził dr Brooke Morriswood, z wydziału Cell and Developmental Biology, Uniwersytetu w Würzburgu. Jego wykłady skupiały się wokół następujących zagadnień:
- znaczenie regularnego czytania publikacji naukowych jako istotna część działalności naukowej;
- analiza części składowych pracy naukowej;
- w jaki sposób zaangażować młodych naukowców do krytycznego czytania prac naukowych;
- jak prowadzić nadzór nad literaturą naukową.
W wykładach uczestniczyło ponad 50 doktorantów i pracowników naukowych MIBMiK. Dr Morriswood udzielił wielu praktycznych wskazówek, przydatnych zarówno przy czytaniu, jak i pisaniu publikacji naukowych. - "Bardzo się cieszę, że Brooke przyjął nasze zaproszenie do poprowadzenia kursu z zakresu krytycznego czytania prac naukowych i jestem pewna, że wszyscy z niego skorzystamy. Wykładom towarzyszą praktyczne warsztaty dla naszych doktorantów, które odbywają się w tym tygodniu - powiedziała prof. Marta Miączyńska, Dyrektorka MIBMiK.
Warsztaty stacjonarne dedykowane były doktorantom i prowadzone przez kierowników laboratoriów MIBMiK: prof. Martę Miączyńską, prof. Matthiasa Bochtlera oraz dr Katarzynę Mleczko-Sanecką. Uczestnicy szkolenia, podzieleni na małe grupy, analizowali i omawiali wybrany artykuł badawczy.
Dr Brooke Morriswood jest kierownikiem na Wydziale Cell & Developmental Biology na Uniwersytecie w Würzburgu, Niemcy. Jest biologiem molekularnym komórki, który interesuje się cytoszkieletem, białkami motorycznymi i handlem błonami.
Ukończył Uniwersytet Cambridge (2002) na kierunku biochemia oraz studia doktoranckie pod kierunkiem Johna Kendricka-Jonesa w Laboratory of Molecular Biology, Cambridge (2006). Studia podoktorskie prowadził w laboratorium Grahama Warrena na Uniwersytecie Yale (2007) oraz w Max F. Perutz Laboratories w Wiedniu (2008-2014). W 2015 roku Brooke został kierownikiem grupy na Uniwersytecie w Würzburgu.
Kurs odbył się dzięki wsparciu projektu MOSaIC.


Wykład Critical Reading of Scientific Papers został zorganizowany i sfinansowany w ramach projektu MOSaIC, który otrzymał dofinansowanie z programu Unii Europejskiej Horyzont 2020 w zakresie badań i innowacji (umowa o dofinansowanie nr 810425).
{gallery}course{/gallery}
Pozytywna pamięć genetyczna, pamięć transkrypcyjna – od czego zależy? Jakie dokładnie czynniki za nią odpowiadają? Ostatnio opublikowany artykuł w czasopiśmie Cellular and Molecular Life Sciences autorstwa naukowców z Laboratorium Biologii Strukturalnej przyczynia się do lepszego zrozumienia pozytywnej pamięci genetycznej.
Jak to możliwe, że po podziale komórki (tzw. mitozie) komórka potomna "pamięta" jaką powinna mieć "tożsamość"? Dlaczego komórka nerwowa nie staje się nagle komórką serca, skoro obie mają takie samo DNA? Za prawidłowy mechanizm utrzymania tej "tożsamości" odpowiada pamięć epigenetyczna, która wprowadza odpowiednie znaczniki genów powodujące, że stają się one aktywne lub wyłączone.
Okazuje się, że proces umieszczania znaczników aktywnych genów (pozytywna pamięć epigenetyczna) jest katalizowany m.in. przez białko KMT2/MLL, obecne w różnych tkankach. Zaburzenia pracy tego białka wprowadzają zamęt i zmiany "tożsamości" komórek, co w konsekwencji najczęściej wywołuje choroby nowotworowe, ale również psychiczne.
Naukowcy z Międzynarodowego Instytutu Biologii Molekularnej i Komórkowej w Warszawie pod kierownictwem prof. Matthiasa Bochtlera chcieli zrozumieć, w jaki sposób białka KMT2/MLL znajdują swoje cele, aby móc wprowadzić znacznik w obrębie aktywnych genów. W najnowszej pracy Stroynowska-Czerwińska i wsp. pokazują, że małe fragmenty tych białek (tzw. domeny) i interakcje między nimi są wystarczające do tego celu. Autorzy udowadniają również, że nawet pojedyncza, związana z nowotworem, mutacja zmiany sensu w obrębie tych domen może znieść specyficzność ich celowania.
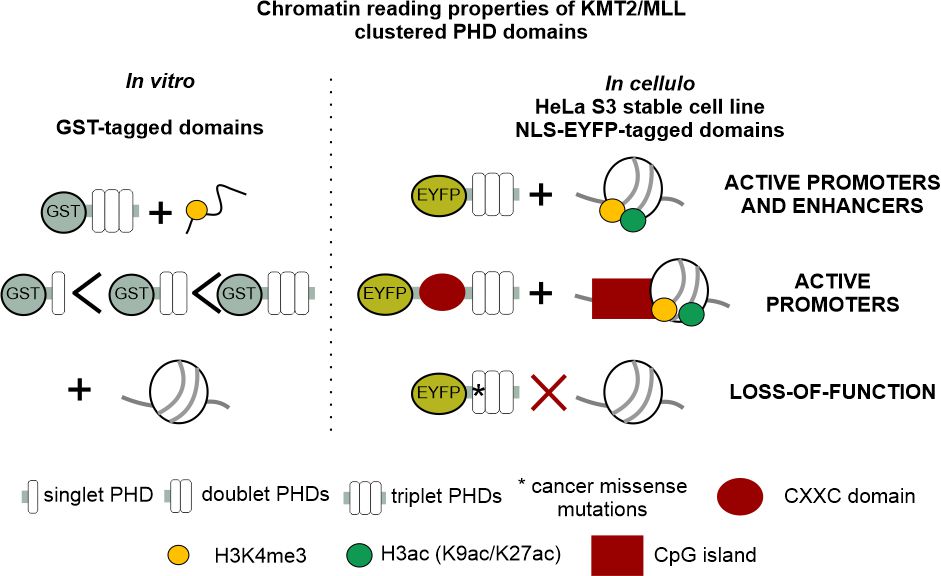
Podsumowując, pamięć genetyczna zależy od pętli sprzężenia zwrotnego, która odpowiada za metylację H3K4, aktywny znacznik chromatyny, na aktywnych promotorach i wzmacniaczach. Do tej pory nie rozumiano, w jaki sposób metylotransferazy KMT2/MLL znajdują swoje cele chromatynowe. Stroynowska-Czerwinska i in. pokazują, że skupione domeny PHD w białkach KMT2/MLL są wystarczające do tego celu. Autorzy wykazali, że znane preferencje promotora lub wzmacniacza poszczególnych metylotransferaz KMT2/MLL można przypisać odpowiednio obecności lub nieobecności w nich domen CXXC. Praca przedstawia pierwszą cało-genomową charakterystykę wiązania domen będacych czytnikami histonów w komórkach. Mutacje genów KMT2/MLL są silnie związane z rakiem. Autorzy pokazują, że nawet pojedyncza związana z rakiem mutacja zmiany sensu w domenach PHD może znieść specyficzność celowania. Dlatego praca ma również implikacje medyczne.”
Artykuł dostępny pod linkiem:
https://link.springer.com/article/10.1007/s00018-022-04651-1
Stroynowska-Czerwinska, A.M., Klimczak, M., Pastor, M. et al. Clustered PHD domains in KMT2/MLL proteins are attracted by H3K4me3 and H3 acetylation-rich active promoters and enhancers. Cell. Mol. Life Sci. 80, 23 (2023). https://doi.org/10.1007/s00018-022-04651-1
To będzie jedno z ważniejszych wydarzeń naukowych w Polsce w 2023 roku! Z radością informujemy, że dziś otworzyliśmy możliwość rejestracji na konferencję Polish RNA Biology Meeting PL - RNA 2023! O szczegółach wydarzenia, programie i zaproszonych gościach opowiadają w krótkim filmie video prof. Andrzej Dziembowski – Przewodniczący Komitetu Organizacyjnego i prof. Gracjan Michlewski – Przewodniczący Komitetu Naukowego, na codzień Kierownicy Laboratoriów w Międzynarodowym Instytucie Biologii Molekularnej i Komórkowej w Warszawie.
Obszar biologii RNA – to dynamicznie rozwijająca się dziedzina nauk przyrodniczych, odnosząca się do zagadnień takich jak: biologia RNA w układach prokariotycznych i eukariotycznych, transkrypcji, przetwarzania i metabolizmu RNA oraz zastosowania RNA w terapii i medycynie.
Głównym celem spotkania jest zebranie w jednym miejscu wybitnych naukowców, specjalistów w zakresie biologii RNA z Polski i ze świata, umożliwienie im wymiany wiedzy i doświadczeń oraz nawiązanie współpracy. Konferencja będzie również znakomitą okazją dla doktorantów i badaczy podoktorskich do zaprezentowania swoich najlepszych projektów badawczych. W wydarzeniu swój udział zapowiedzieli światowej sławy specjaliści: prof. Lori Passmore, prof. Alfredo Castello, prof. Andrea Rentmeister oraz prof. Witold Filipowicz.
Link do rejestracji:https://pl-rna.iimcb.gov.pl/
Przewodniczącym Komitetu Naukowego jest prof. Gracjan Michlewski, Kierownik Laboratorium Oddziaływań RNA-Białko - Centrum Dioscuri w MIBMiK.
Członkami Komitetu Naukowego są: prof. Sebastian Glatt, Małopolskie Centrum Biotechnologii, Uniwersytet Jagielloński, prof. Jacek Jemielity, Uniwersytet Warszawski, prof. Kinga Kamieniarz-Gdula, Uniwersytet im. A. Mickiewicza w Poznaniu, prof. Elżbieta Kierzek, Instytut Chemii Bioorganicznej PAN w Poznaniu oraz prof. Joanna Kufel, Uniwersytet Warszawski.
Przewodniczącym Komitetu Organizacyjnego jest prof. Andrzej Dziembowski, Kierownik Laboratorium Biologii RNA - Grupa ERA Chairs w MIBMiK.
Spotkanie organizowane jest w ramach projektu MOSaIC, finansowanego z programu Horizon2020 ERA Chairs.
Więcej informacji: https://pl-rna.iimcb.gov.pl/
To wspaniały news na początek roku! Natalia Szulc z Laboratorium Metabolizmu Białek otrzymała stypendium Fulbright’a! Serdecznie gratulujemy tego sukcesu! Cieszymy się tym bardziej, że Natalia jest pierwszą osobą z naszego Instytutu, która otrzymała to prestiżowe stypendium!
Fulbright Junior Research Award to stypendium dla doktorantów na wyjazd na uniwersytet, do instytutu badawczego lub organizacji pozarządowej w Stanach Zjednoczonych w celu realizacji projektu związanego z tematem pracy doktorskiej.
Dzięki stypendium Fulbrighta Natalia zdobędzie doświadczenie w rozwoju leków opartych na technologii ukierunkowanej degradacji białek. Są to nowatorskie i obiecujące terapie oparte na manipulacji systemem ubikwityna-proteasom w celu selektywnej degradacji wybranych białek, co pozwala na walkę np. z chorobami nowotworowymi poprzez sterowanie usuwaniem białek sprzyjających powstawaniu guzów.
Natalia będzie realizować projekt badawczy związany z modelowaniem obliczeniowym degraderów białek w Dana-Farber Cancer Institute, instytucie posiadającym światowej sławy doświadczenie w technologii ukierunkowanej degradacji białek.












